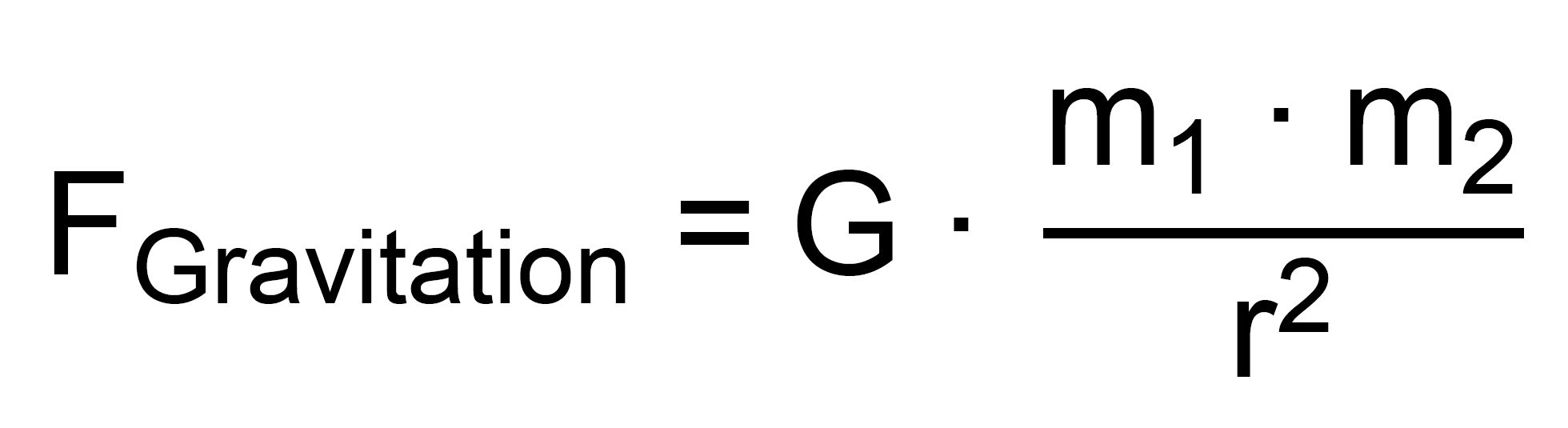|
Das Coulombsche Gesetz Einführung Das Coulombsche
Gesetz ist nach dem Physiker Charles
Augustin de Coulomb (1736-1806) benannt, der dieses Gesetz formuliert hat. Es geht dabei um die Kräfte, die zwischen zwei Kugelladungen im Ab- stand r herrschen. Das Gesetz ähnelt sehr dem Gravitationsgesetz. Die experimentelle Herleitung ist recht komplex, so dass wir hier zu- nächst eine theoretische Herleitung vornehmen. Im Anschluss werden allerdings mehrere mögliche Experimente vorgestellt und auch Mess- werte ausgewertet. Theoretische
Herleitung Um die theoretische
Herleitung zu verstehen, muss man sich zunächst mit dem Kapitel
Flächenladungsdichte beschäftigen und den Zusam- menhang zur Feldstärke
kennen. Da es
sich um Kugelladungen handelt, beschäftigen wir uns am An- fang mit
dem radialsymmetrischen
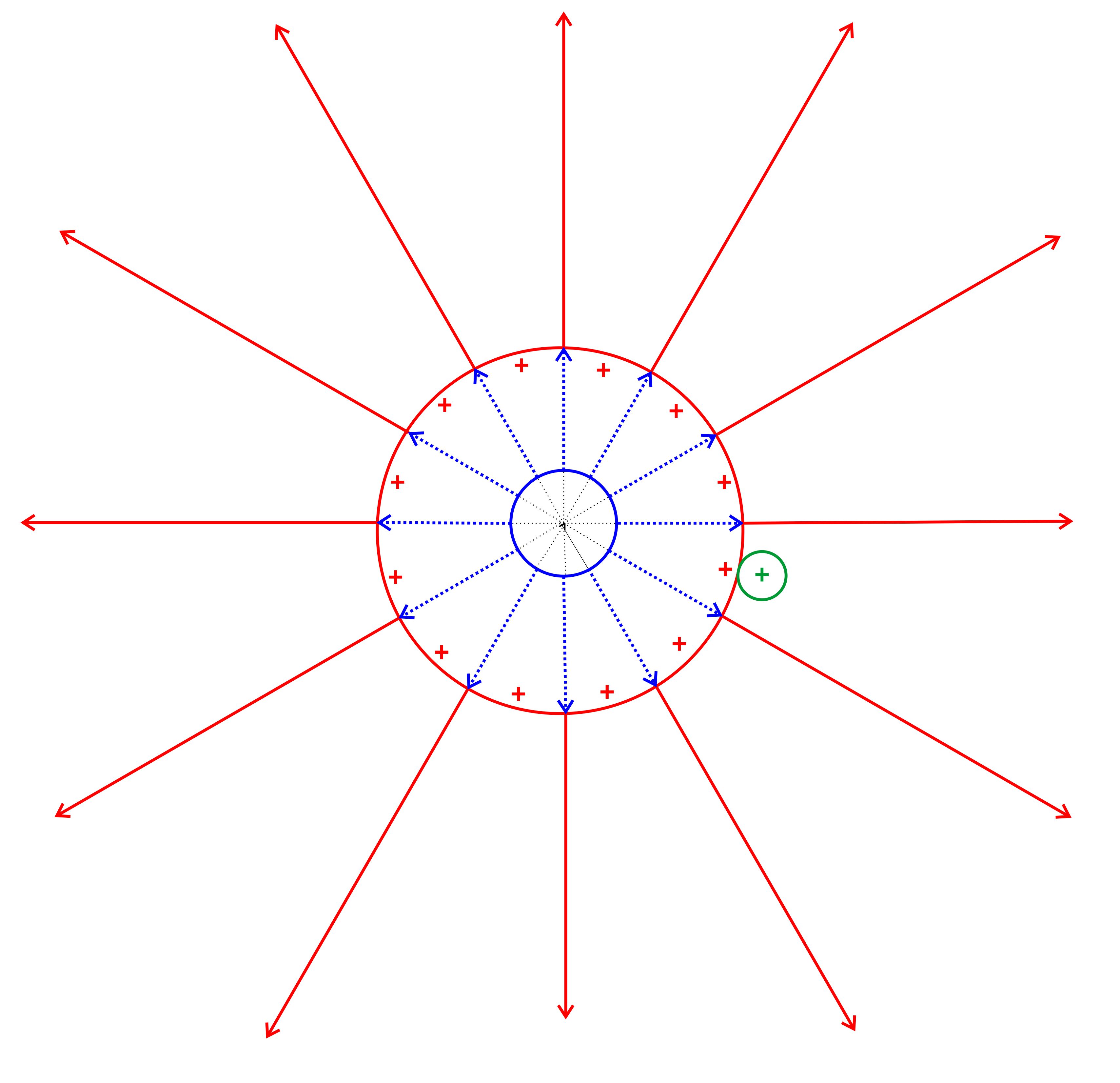
E-Feld. Hierzu folgende Abbildung.
Wir
konzentrieren uns zunächst auf die rote positive Kugel mit ihrem Radialfeld,
deren Feldlinien rot eingetragen sind. Die Ladungen be- finden
sich alle auf der Oberfläche wegen der gegenseitigen Ab- stoßung.
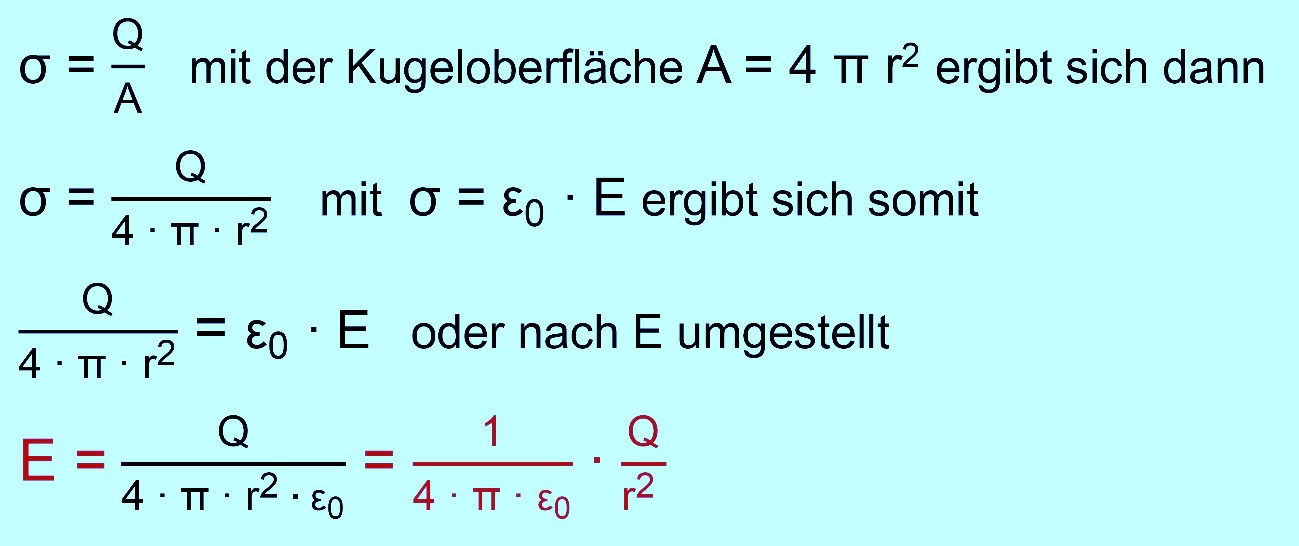
Aus der Flächenladungsdichte der Kugel lässt sich schnell eine
Formel für die elektrische Feldstärke des Radialfeldes gewinnen. Es gilt
nämlich:
Für die
Kraft zwischen „grüner“ und „roter“ Ladung gilt somit aufgrund
der Definition
der Feldstärke:
Nun wird
bei der Herleitung ja eine „grüne“ Ladung auf der Oberfläche der
„roten“ Ladung angenommen, damit man die Flächenladungs- dichte
benutzen kann, wobei „r“ jetzt der Radius der „roten“ Kugel ist. Man kann
somit über σ die Feldstärke auf der Oberfläche bestimmen und
damit dann die Kraft auf der Oberfläche. Wenn man
jetzt die große Kugel kleiner macht (s. „blaue“ Kugel) er- kennt
man aber, dass sich an dem Feldlinienbild und somit auch der Feldliniendichte
nichts ändert, d.h. die Formel für E und F gelten weiterhin!
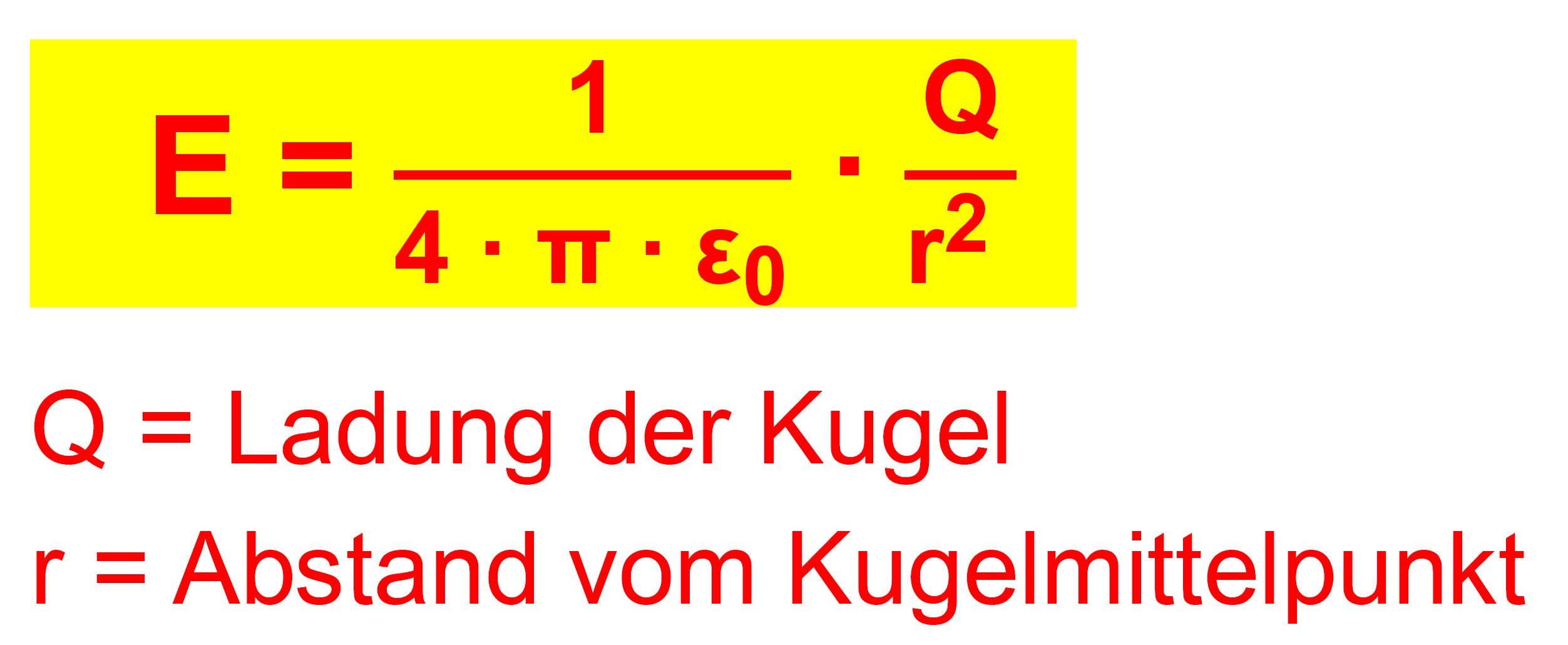
Wir müssen nur jetzt „r“ nicht als Radius, sondern als Ab- stand
vom Mittelpunkt verstehen. Man kann
also die Ergebnisse allgemeiner deuten. Die Formeln also die Radialfeldstärke E im Abstand r vom Mittelpunkt der (die Größe der Kugel spielt ja keine Rolle). F gibt die Kraft zwei geladenen Kugeln an, deren Mittelpunkte einen Abstand „r“ auf- weisen.
Man
sieht sofort die Ähnlichkeit mit dem Gravitationsgesetz,
dass den gleichen
Aufbau aufweist. Es gilt dort:
Experimentelle
Herleitung des Coulombschen Gesetzes Wie oben
schon erwähnt, hat die experimentelle Herleitung gewisse Tücken.
Es gibt sehr viele verschiedene Möglichkeiten der Versuchs- durchführung. Deshalb habe ich diesem Thema ein eigenes Kapitel
gewidmet,
welche man unter folgendem
LINK: Experimentelle Herleitung
- zurück zur Übersicht „Felder“ |